Artigo encontrado na Revista de Ciências Farmacêuticas Básica e Aplicada. (Rev Ciênc Farm Básica Apl., 2010;31(1):15-23 ISSN 1808-4532)
Autor: Pires, A.P.S.1 ; Oliveira, C.D.R.1 *; Yonamine, M.1 1 Departamento de Análises Clínicas e Toxicológicas, Faculdade de Ciências Farmacêuticas, Universidade de São Paulo, SP, Brasil Autor correspondente: Carolina Dizioli Rodrigues Oliveira – Faculdade de Ciências Farmacêuticas – Av. Prof. Lineu Preste, 580-B13B – Cidade Universitária – CEP.05508-900, São Paulo, SP – tel: (11) 3091-2194 – e-mail: cdro@usp.br Recebido 04/08/2009 / Aceito 11/03/2010
Autor correspondente: Carolina Dizioli Rodrigues Oliveira – Faculdade de Ciências Farmacêuticas – Av. Prof. Lineu Preste, 580-B13B – Cidade Universitária – CEP.05508-900, São Paulo, SP
RESUMO
A ayahuasca é uma bebida psicoativa originariamente utilizada em rituais de tribos indígenas da região amazônica. Esta bebida é preparada pela infusão de caules da Banisteriopsis caapi Morton, que contém β-carbolinas que são inibidoras da monoaminoxidase (MAO), e de folhas da Psychotria viridis Ruiz & Pavón, que contém o alucinógeno N,N-dimetiltriptamina (DMT). A enzima MAO degrada a DMT no fígado e intestino. No Brasil, a ayahuasca tem sido incorporada em rituais de grupos sincréticos religiosos e seu uso dentro do contexto religioso é amparado por lei federal. Atualmente, esses grupos têm se espalhado na Europa e Estados Unidos, chamando a atenção de pesquisadores internacionais quanto aos efeitos da ayahuasca. Estudos têm indicado que a ayahuasca poderia ter aplicações terapêuticas como no tratamento da farmacodependência e até sugerem seu uso seguro por adultos sadios. Entretanto, poucos estudos têm sido conduzidos para melhor avaliação de suas propriedades. O objetivo do artigo é mostrar uma revisão geral da história até as recentes descobertas envolvendo a farmacologia e a toxicologia da ayahuasca.
INTRODUÇÃO
A ayahuasca, também conhecida pelos nomes de caapi, daime, yajé, natema, vegetal e hoasca, é uma bebida composta pela associação de duas plantas primordiais: o caule da Banisteriopsis caapi Morton e as folhas da Psychotria viridis Ruiz & Pavón (Callaway & Grob, 1998; Santos et al., 2006). Originalmente, era utilizada por grupos indígenas associados ao xamanismo e por vegetalistas curandeiros que praticavam a medicina popular à base de extratos vegetais. A palavra ayahuasca é originária da língua quéchua e quer dizer: “aya”: “pessoa morta, espírito” e “waska” que significa “corda, liana, cipó”; logo, traduzindo-se para o português ficaria “corda dos mortos” (Luna, 1986; Tupper, 2002).
A combinação do caule com as folhas forma uma associação sinérgica, pois a B. caapi possui β-carbolinas: harmalina (HRL), harmina (HRM) e tetraidro-harmina (THH), inibidoras reversíveis da enzima monoaminoxidase (MAO) e a P. viridis, contém a N,N-dimetiltriptamina (DMT), que é um potente alucinógeno, também metabolizada pela MAO. Dessa forma, a ingestão da bebida proporciona aumento nas concentrações de serotonina e torna biodisponível a DMT por via oral, provocando ação alucinógena (Callaway & Grob, 1998). O uso da ayahuasca é difundido em vários países da América do Sul, tais como Peru, Bolívia, Colômbia, Brasil, Venezuela e Equador e nos últimos anos, grupos de seguidores dessas religiões brasileiras têm se estabelecido nos Estados Unidos e em vários países europeus, incluindo a Alemanha, Inglaterra, França e Espanha (Riba et al., 2003; Tupper, 2008). Embora tenha existido toda essa expansão no consumo, é apenas no Brasil que se desenvolveu o uso ritualístico em populações não-indígenas, centralizadas em rituais religiosos.
Entretanto, o Brasil é o único país a ter o uso da ayahuasca para fins religiosos amparado por lei, a exemplo do que ocorre com o uso do peyote (Lophophora williamsii, um cacto que contém mescalina) pela Native American Church nos Estados Unidos (Riba et al., 2001). O uso religioso da ayahuasca foi reconhecido como prática legal no Brasil pelo Conselho Nacional Antidrogas, em Resolução de 04 de novembro de 2004 (Conselho Nacional Anti-drogas, 2004). Entretanto, apesar da longa história e tradição do uso indígena e a incorporação dessa prática em grupos religiosos ter se expandido mundialmente nos últimos anos, relativamente poucas informações pré-clínicas e clínicas foram acumuladas no sentido de fornecer uma base científica consistente para afirmar que o uso da ayahuasca é seguro ou não (Barker et al., 2001; McKenna, 2004). Essa falta de informação abre margem para especulações e controvérsias sobre os possíveis efeitos indesejados da exposição aos alcalóides presentes nessa bebida. Desta forma, o objetivo do presente trabalho foi fazer uma revisão dos aspectos farmacológicos e toxicológicos da ayahuasca encontrados na literatura científica.
HISTÓRICO
No mundo todo, estima-se que exista cerca de meio milhão de espécies vegetais. Destas, mais de 450 espécies de plantas e cogumelos com potencial de abuso podem ser definidas como psicoativas, dos quais cerca de 120 possuem propriedades alucinógenas. Plantas alucinógenas estão entre as mais antigas drogas usadas e abusadas pelo homem. Durante séculos, a utilização destas plantas era associada somente à religião, magia e medicina. Entretanto, as mesmas características dessas plantas que levaram à sua incorporação em importantes rituais e tradições espirituais, também resultaram em seu abuso (Cunningham, 2008).
Em 1845, Jacques Moreau publicou o primeiro texto sobre alucinógenos, onde observou que alguns compostos permitiam a transformação de pensamentos em experiências sensoriais. Em 1924, o alemão Loius Lewin, creditado como estudioso pioneiro, antropólogo e “avô” da investigação científica em toxicologia e psicofarmacologia, escreveu a monografia intitulada “Phantastica – um estudo clássico sobre o uso e abuso de plantas que alteram a consciência”, e em sua obra já citava as propriedades alucinógenas da ayahuasca (Cunningham, 2008).
Nos últimos anos, o uso da ayahuasca tem se expandido além da cultura indígena e vem sendo utilizada em alguns movimentos sincréticos religiosos, que buscam um meio de facilitação do autoconhecimento e introspecção (Yritia et al., 2002; Carlini, 2003). Dentre esses grupos, os que mais se destacam são: o Santo Daime, a União do Vegetal (UVD) e a Barquinha (Labate, 2004). Essas comunidades religiosas foram criadas após o início do ciclo da borracha em 1930, período de urbanização da região norte do país e de grande interação entre seringueiros e indígenas de tribos xamânicas (Chauí, 2000). Nesse período, em Rio Branco, capital do Acre, Raimundo Irineu Serra, ex-seringueiro, migrante do Maranhão e conhecido “curador”, após ter experimentado a bebida oferecida por pessoas que tiveram contato com costumes indígenas, começou a ter visões que mudaram seu comportamento e qualidade de vida (Goulart, 2004).
Iniciava, então, um culto de comunidade que possuía como ponto básico a ingestão da ayahuasca denominada aqui de Santo Daime, que daria também origem ao nome da religião. O culto daimista foi um marco rompedor da antiga tradição de consumo da bebida sem contexto por parte das tribos indígenas para uma nova forma, contextualizada e bem definida, com objetivos e regras estipuladas. Por volta de 1945 foi fundada por Frei Daniel Pereira de Mattos a Barquinha, também em Rio Branco, Acre. Talvez esta seja a linha ayahuasqueira mais eclética das três, possuindo influências de práticas religiosas, tais como catolicismo, xamanismo indígena e religiões afro-brasileiras (Goulart, 2004; Labate, 2004).
Na década de 1960, através do “mestre” José Gabriel da Costa, forma-se a União do Vegetal (UDV) com sede em Planaltina (Brasília-DF). Esta organização possui uma doutrina cristã-reencarnacionista, permeada por elementos do espiritismo kardecista e de outras manifestações religiosas urbanas. Existem hoje cerca de cinco mil pessoas ligadas à UDV em diversos locais do país (Labigaline, 1998; Labate, 2004).
As três principais vertentes (Santo Daime, UDV e Barquinha) têm em comum o fato de pertencerem a uma mesma tradição de religiosidade não-indígena de consumo da ayahuasca no Brasil. Assemelham-se com relação ao preparo do chá, à cerimônia e às regras para adesão dos membros. Porém, cada uma delas possui diferenças de contexto religioso e social significativas entre si, o que veio a originar cisões em relação aos grupos originais (Labate, 2004; Tupper, 2008).
Apesar da longa história e tradição do uso indígena, e a incorporação dessa prática em grupos religiosos ter se expandido mundialmente, relativamente poucas informações pré-clínicas e clínicas foram acumuladas no sentido de fornecer uma base científica consistente para afirmar que o uso da ayahuasca é seguro (Barker et al., 2001; Mckenna, 2004). Essa falta de informação abre margem para especulações e controvérsias sobre os possíveis efeitos indesejados da exposição aos alcalóides presentes nessa bebida.
AYAHUASCA E PRINCIPAIS CONSTITUINTES QUÍMICOS
A ayahuasca consiste, geralmente, na cocção de duas plantas: as cascas e caules da liana da família Malphighiaceae Banisteriopsis caapi, junto com as folhas do arbusto da família Rubiaceae Psycotria viridis (Callaway et al., 1994; Liwszyc et al., 1992; Mckenna et al., 1984; Mckenna, 2004; Ott, 1994). Entretanto, outras plantas de diversas famílias podem ser adicionadas no preparo do chá (Ott, 1994). Ott (1994) cita 98 espécies de 39 famílias de plantas que podem ser adicionadas à ayahuasca.
Psychotria viridis foi primeiramente descrita por Ruiz & Pavón em 1779 (Aranha et al., 1991). A espécie, possui o alcalóide N,N-dimetiltriptamina (DMT) em suas folhas. Psychotria é um grande gênero de arbustos e pequenas árvores encontrados em regiões tropicais de todo o mundo (incluindo cerca de 1.400 espécies) e sua taxonomia é um pouco complexa. Muitas outras espécies são morfologicamente semelhantes à Psychotria viridis e algumas dessas espécies são provavelmente usadas no preparo da ayahuasca (Blackledge & Taylor, 2003). Podem também ser utilizadas outras espécies do gênero Psychotria, tais como Psychotria cartagenensis, ou Diplopterys cabrerana (Mckenna et al., 1984).
As aminas indólicas psicoativas DMT e seus análogos bufotenina e 5-MeO-DMT, também são constituintes de rapés e chás preparados a partir de diferentes espécies vegetais que crescem em várias regiões da América. Nos Estados Unidos, concentrações apreciáveis de DMT são encontradas em extratos de Phalaris (Phalaris arundinacea, Phalaris tuberosa e Phalaris aquatica, esta última encontrada também no Canadá). Estas espécies são muito utilizadas para elucidação da biogênese das indolalquilaminas e são geralmente encontradas em campos sem cultivo e em calçadas rachadas. Desmanthus illinoensis também possui DMT em suas raízes (Thompson et al., 1987).
Há muitas outras fontes botânicas de DMT na região da América do Sul. Essa substância pode ser extraída de sementes de Anadenanthera peregina ou de cascas de caules de Virola spp., Piptadenia, Mimosa hostilis, Diplopterys cabrerana (syn. Banisteriopsis rusbyana) e Lespedeza bicolor (Thompson et al., 1987).
Banisteriopsis caapi foi classificada por Morton em 1931 (Aranha et al., 1991). É conhecida como mariri e é um cipó ou parreira gigante pertencente à família Malpighiaceae sendo nativa das zonas tropicais da América do Sul e Antilhas. Possui alcalóides β-carbolínicos que são potentes inibidores reversíveis da MAO-A. As principais β-carbolinas são harmina (HRM), também conhecida como telepatina; harmalina (HRL) e tetraidro-harmina (THH) (Callaway & Grob, 1998).
As concentrações de β-carbolinas encontradas em B. caapi variam de 0,05% a 1,95% de peso seco, enquanto em P. viridis as concentrações de alcalóides estão na faixa de 0,1 a 0,66% de peso seco (McKenna et al., 1984; McKenna, 2004).
As concentrações de alcalóides na bebida ayahuasca são maiores que as encontradas nas plantas utilizadas para seu preparo (Mckenna, 2004). Na ayahuasca de origem peruana, McKenna et al. (1984) verificaram que uma dose de 100 mL continha cerca de 60 mg de DMT, 41 mg de harmalina, 467 mg de harmina e 160 mg de tetraidro-harmina. Em outro experimento, Callaway et al. (1996) obtiveram os seguintes resultados de concentração de alcalóides presentes no chá utilizado por um grupo religioso do Brasil: 0,24 mg/mL de DMT, 0,20 mg/mL de harmalina, 1,70 mg/mL de harmina e 1,07 mg/mL de tetraidro-harmina. Isso significa que uma dose típica de 100 mL dessa bebida contém 24 mg de DMT, 20 mg de harmalina, 170 mg de harmina e 107 mg de tetraidroharmina. As diferenças nas concentrações e proporções dos alcalóides encontrados nos chás de ayahuasca estão provavelmente relacionadas com o método de preparação, a quantidade e proporção das partes das plantas empregadas em seu preparo (Mckenna, 2004).
Mais recentemente, Gambelunghe et al. (2008) encontraram 0,24 mg/mL de DMT; 0,06 mg/mL de HRL e 0,34 mg/mL de HRM. Pires et al. (2009) também determinaram as concentrações de alcalóides em diferentes preparações de ayahuasca, obtendo-se os seguintes teores: 0,31 a 0,73 mg/mL de DMT; 0,21 a 0,67 mg/mL de THH; 0,64 a 1,72 mg/mL de HRL e 0,37 a 0,83 mg/mL de HRM.
FARMACOCINÉTICA DOS ALCALÓIDES
Estudos de farmacocinética dos alcalóides presentes na ayahuasca são escassos na literatura. Callaway et al. (1999) relataram resultados da medida de concentração plasmática de voluntários que ingeriram a bebida durante o andamento de uma cerimônia religiosa. A concentração plasmática máxima (Cmx) de DMT encontrada foi de 15,8 ng/mL e ocorreu 107 minutos após a ingestão. A meia-vida foi de 259 minutos. A Cmx de tetraidro-harmina de 91 ng/mL foi alcançada em 174 minutos e apresentou meia-vida mais prolongada (532 min). Em relação à harmina e harmalina, a Cmx foi de 114,8 e 6,3 ng/mL, respectivamente obtida após 102 e 145 minutos. A harmalina foi detectada em apenas 6 indivíduos e a DMT em 12 dos 15 voluntários, provavelmente devido às baixas concentrações desta substância no chá, por diferenças individuais na absorção e metabolismo ou devido a êmese causada pela ingestão da ayahuasca. A meia-vida (t1/2) da harmina foi de 115,6 minutos enquanto a t1/2 da harmalina não pôde ser determinada. Os efeitos subjetivos foram avaliados através da Escala de HRS (Hallucinogen Rating Scale), que permite medir níveis de alucinação. A duração desses efeitos foi coincidente com os níveis de alcalóides presentes no plasma, variando entre visualização de imagens coloridas com olhos fechados, modificação dos processos perceptivos, cognitivos e afetivos.
Em outro estudo conduzido por Riba et al. (2003), foram administradas doses de 0,6 e 0,85 mg de DMT/kg de peso corpóreo na forma de cápsulas de ayahuasca seca, em oito voluntários com histórico prévio de uso de psicodélicos. A ayahuasca produziu significantes efeitos subjetivos, com intensidade máxima alcançada entre 1,5 a 2 horas após a ingestão. A concentração plasmática máxima de DMT após a menor e a maior dose foram de 12,14 ng/mL e 17,44 ng/mL, respectivamente. O tempo que se obteve a Cmx coincidiu com o pico de intensidade de efeitos subjetivos, tais como cognição, sensibilidade a reações emocionais, percepção visual, experiências auditivas, gustativas e olfativas; que foram medidos através de Escala Visual Analógica, Escala de HRS e questionário de auto-avaliação.
Alguns métodos analíticos para determinação dos alcalóides da ayahuasca em amostras biológicas têm sido publicados na literatura. A DMT tem sido quantificada em plasma por cromatografia em fase gasosa com detector de nitrogênio-fósforo (GC-NPD), enquanto β-carbolinas são determinadas por cromatografia líquida de alta eficiência (HPLC) com detector de fluorescência (Callaway et al., 1996; Yritia et al., 2002). Mais recentemente, um método foi desenvolvido para determinação de triptaminas alucinogênicas em sangue e urina por cromatografia em fase gasosa acoplada à espectrometria de massa (GC-MS) e cromatografia líquida acoplada à espectrometria de massa (LC-MS) (Vorce & Sklerov, 2004).
A DMT, quando administrada pela via pulmonar (fumada) ou pela via intravenosa, foi capaz de produzir efeitos alucinógenos, quase imediatos. Uma simples inalação produziu de cinco a dez minutos de “viagem”, que durou em torno de 30 minutos, caracterizada por alucinações multicoloridas. Não há estudos sobre a toxicologia ou a cinética da DMT fumada. Já para a forma injetável, com doses de 0,2 a 0,4 mg/kg, foram observados quase instantaneamente o aparecimento de náuseas, vômitos, taquicardia e de efeitos subjetivos tais como alterações do estado emocional e afetivo, modificação da sensação de tempo e das sensações do próprio corpo, sinestesia, medo e insônia, sendo que as concentrações sanguíneas associadas com as visões foram medidas em 32-204 ng/mL, depois de uma dose de 0,4 mg/kg (Laing & Siegel, 2003; Shannon, 2003).
Já para o chá, o tempo para início dos efeitos é de aproximadamente uma hora após a ingestão. Esses efeitos, que são menos intensos que os produzidos pela DMT parenteral ou fumada, duram aproximadamente quatro horas (Brito, 2004).
FARMACODINÂMICA DO ALCALÓIDES
O termo alucinógeno é utilizado para agrupar uma categoria abrangente de substâncias psicoativas, variando entre canabinóides, ecstasy (MDMA; 3,4- metilenodioximetanfetamina), dietilamida do ácido lisérigo (LSD), psilocibina, dimetiltriptmamina (DMT), mescalina, 2,5 dimetoxi-4-metil anfetamina (DOM), entre outras, caracterizando-se por substâncias que promovem efeitos que incluem sintomas somáticos, de percepção e psíquicos (Nichols, 2004).
Os efeitos subjetivos similares aos desses compostos são observados na exposição à ayahuasca e podem ser exemplificados na área somática por náuseas, vômitos, tremores, tonturas, debilidade, contratura muscular, hiperreflexia, dores generalizadas, taquicardia (Callaway & Grob, 1998). No plano psíquico, verificam-se profundas e rápidas alterações dos estados emocionais: o indivíduo vai da depressão à euforia em poucos segundos. Pânico, apatia, alterações na memória e no pensamento, despersonalização e hipersugestabilidade, medo, insônia e sensação de morte iminente também podem ser observados. No plano perceptivo-sensorial observam-se distorções de tempo e espaço, estranhas sensações corporais, alterações nas percepções de formas, cores, sons, sinestesias e alucinações com alterações auditivas, olfativas e visuais (Shannon, 2003).
A DMT é estruturalmente semelhante ao neurotransmissor serotonina e age ligando-se a receptores 5-HT1a , 5HT1b , 5-HT2a e 5HT2c existentes no sistema nervoso central (Yritia et al., 2002). A serotonina (5-HT) é um dos principais neurotransmissores do sistema nervoso central. É sintetizada a partir do aminoácido essencial triptofano, e atua como regulador da função da musculatura lisa nos sistemas cardiovascular e gastrintestinal, na glândula pineal e nas plaquetas (Goodman & Gilman, 2007).
Os neurônios serotoninérgicos cerebrais estão envolvidos em diversas funções fisiológicas tais como sono, humor, sensação de dor, controle da temperatura e regulação da pressão arterial e em condições patológicas, tais como enxaqueca, ansiedade e depressão (Goodman & Gilman, 2007). No sistema cardiovascular, os principais efeitos são contração do músculo liso e potente vasoconstrição, que justifica possíveis aumentos na pressão arterial, devido ao aumento na resistência periférica (Costa et al., 2005).
Essa ação agonista serotoninérgica da DMT produz uma série de alterações cognitivas, sensoriais e emocionais momentâneas quando administrada por via parenteral. As modificações na percepção parecem ser bastante intensas, porém com um período de tempo bastante curto em sua duração (Strassman et al., 1994; Pomilio et al., 1999; Freedland & Mansbach, 1999).
Quando administrada por via oral, entretanto, tem sido demonstrada a perda de atividade da DMT devido à degradação de primeira passagem realizada pela enzima monoaminoxidase-A (MAO-A) periférica (Ott, 1994). Conjuntamente, a ayahuasca contém β-carbolinas, como a harmina, a harmalina e a tetraidro-harmina, presentes na B. caapi. A harmina e a harmalina e em menor extensão, a tetraidro-harmina, são potentes inibidores da MAO, fato que explica as propriedades psicoativas da bebida. Desta forma, as β-carbolinas impediriam a degradação da DMT no trato gastrintestinal, possibilitando que o fármaco fique disponível para ser absorvido (Riba et al., 2003). De fato, verificou-se que a DMT é inativa após administração oral de doses até 1000 mg, enquanto que em doses parenterais de 25mg já se observam alguns efeitos neurocomportamentais (Strassman & Qualls, 1994; Mckenna, 2004).
As β-carbolinas, por si mesmas, também poderiam contribuir com os efeitos psicoativos da ayahuasca, bloqueando a MAO no cérebro e inibindo fracamente a recaptação de serotonina, fenômenos que aumentariam os níveis do neurotransmissor na fenda sináptica (Cazenave, 2000; Callaway et al., 1999). Entretanto, as quantidades de β-carbolinas presentes numa dose de ayahuasca estão bem abaixo do limiar de sua atividade alucinogênica própria, que são de 300 à 500 mg para HRL e THH e de 100 mg para HRM. Por outro lado, estão acima do limiar para atividade como inibidora da MAO (Brito, 2004).
A seletividade das β-carbolinas para MAO-A sobre a MAO-B (baixa afinidade à MAO no fígado comparada com a MAO no cérebro) pode explicar porque não há relatos de crises hipertensivas associadas com a ingestão da ayahuasca em combinação com alimentos contendo tiramina (Callaway et al. 1999).
Na Figura 1 são apresentadas as estruturas químicas da DMT e as principais β-carbolinas presentes na ayahuasca, assim como a estrutura química do neurotransmissor serotonina, ilustrando suas similaridades químicas.
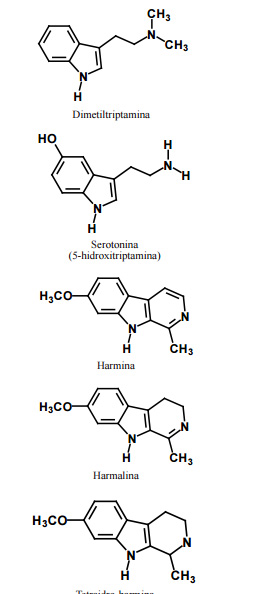
Figura 1 – Estruturas químicas dos principais alcalóides presentes na ayahuasca e do neurotransmissor serotonina.
A DMT, a triptamina e a 5-hidroxi-N,N-dimetiltriptamina (bufotenina) também foram reportadas como constituintes normais da urina e sangue humanos (Franzen & Gross, 1965). A DMT endógena é gerada a partir do aminoácido essencial à alimentação: o triptofano; e a reação (Figura 2) é catalisada graças à ação de duas enzimas: a aminoácido aromático descarboxilase (AADC) (1), que descarboxila o triptofano formando triptamina, e a indoletilamina-N-metiltransferase (INMT) (2), que transfere grupamentos metil do S-adenosilmetionina (SAM) para a triptamina, gerando primeiramente N-metiltriptamina, e em seguida DMT (Jacob & Presti, 2005).
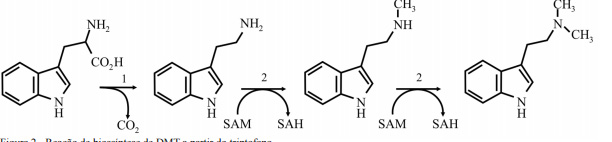
Figura 2 – Reação de biossíntese de DMT a partir do triptofano.
Logo após a descoberta de DMT endógeno em humanos, alguns pesquisadores começaram a analisar correlações entre o aumento dos níveis de DMT em fluidos humanos e a esquizofrenia. Estudos na área descreveram um aumento na excreção urinária de DMT em pacientes esquizofrênicos (Jacob & Presti, 2005).
POSSÍVEIS APLICAÇÕES TERAPÊUTICAS DA AYAHUASCA
Embora existam poucas informações sobre a ação farmacológica em indivíduos que tomam ayahuasca ou sobre a eficácia de suas possíveis aplicações clínicas, há evidências de que a ayahuasca forneça benefícios somados a suas qualidades psicoterapêuticas (Stuckey et al., 2005).
Grob et al. (1996) realizaram avaliações psiquiátricas (n=30) em adultos que faziam uso da ayahuasca no contexto religioso (UDV), comparados com indivíduos que não usavam ayahuasca (grupo controle). Observou-se que esses indivíduos faziam intenso uso de álcool anteriormente e tiveram completa abstinência após a afiliação à UDV. Esses indivíduos também apresentaram diminuição ou ausência de reações crônicas de raiva, agressão, ansiedade, ressentimento e alienação.
As informações relacionadas ao uso de álcool podem ter sido prejudicadas uma vez que a UDV proíbe que seus membros usem qualquer substância psicoativa. Entretanto, os outros parâmetros avaliados como agressão e a procura pela novidade diminuíram significativamente no grupo de usuários de ayahuasca quando comparados com grupo controle e também quando comparados com resultados de outro estudo realizado com usuários de LSD – ácido lisérgico (Halpern & Pope, 1999).
Doering-Silveira et al. (2005a) avaliaram neuropsicologicamente adolescentes (n=84) que usavam ayahuasca no contexto religioso, comparando-os com adolescentes que nunca fizeram uso de ayahuasca (grupo controle). A avaliação neuropsicológica incluiu testes de velocidade de atenção, pesquisa visual, velocidade psicomotora, habilidade verbal e visual, flexibilidade mental e memória. Os resultados mostraram não haver diferença entre os dois grupos para os parâmetros avaliados.
Outro estudo realizou-se uma avaliação psiquiátrica, verificando-se escalas de depressão, ansiedade, uso de álcool e problemas de atenção em adolescentes (n=80) que usavam ayahuasca em comparação a um grupo de adolescentes que não usava (controle). A avaliação mostrou diferenças mínimas entre os grupos, havendo uma tendência a menores sintomas de ansiedade e menor déficit de atenção no grupo que usava ayahuasca (Doering-Silveira et al., 2005).
Mais um estudo, com o mesmo delineamento, também direcionado a avaliação em adolescentes, investigou experiências relacionadas ao uso de substâncias psicoativas. Os resultados obtidos mostraram que não houve diferença estatisticamente significante, porém houve uma proporção maior de relato de uso recente de álcool (65,1% para o grupo controle e 30,5% para o grupo de adolescentes que usava ayahuasca), mostrando a importância da afiliação religiosa como fator protetor em relação ao uso de álcool (Da Silveira et al., 2005).
Através do artigo de revisão de McKenna (2004), observa-se que a ayahuasca possui características que indicam que ela pode apresentar potencial terapêutico: o uso da mesma por tribos remotas a um período de tempo bastante longo e também o fato de apresentar histórico positivo de recuperação no tratamento de indivíduos usuários de álcool e outras substâncias de abuso.
Além destes, há também a possibilidade da ayahuasca atuar regularizando os índices de serotonina em condições de defasagem da modulação a longo prazo. Cogita-se também que possa ter efeitos imuno-modulatórios significantes. Há relatos inclusive de remissão de cânceres e outros problemas sérios relacionados, através do uso regular do chá (McKenna, 2004).
Todos os efeitos terapêuticos observados com o consumo de ayahuasca necessitam de estudos clínicos complementares. Muitas questões relacionadas a uma melhor compreensão dos efeitos da ayahuasca devem ser respondidas com estudos pré-clínicos in vitro e em modelos animais. O resultado desses estudos será, então, útil para o delineamento de subseqüentes estudos clínicos (McKenna, 2004).
ASPECTOS TOXICOLÓGICOS
O critério de letalidade aguda numa única dose em animais de experimentação é uma estimativa extremamente limitada de extrapolação de toxicidade humana, pois não se levam em consideração variáveis como diferenças interespécies, doses repetidas, condições ambientais, estado prévio de saúde e fatores fisiológicos. Apesar disso, a influência que variáveis podem ter numa relação doseresposta estabelecida não pode esconder o fato de que a DL50 (dose letal média, representando a morte de 50% de um total estabelecido) é uma dose claramente definida, reproduzível e importante indicador de toxicidade. Uma extrapolação simples da letalidade do DMT de informações obtidas de camundongos para humanos foi feita. Uma regra tradicional para escalar diferenças desconhecidas entre espécies humanas e não-humanas é simplesmente assumir que humanos são 10 vezes mais sensíveis que roedores. Quando há ausência de informações sobre a DL50 oral de uma substância, como no caso do DMT, deve-se assumir que humanos são 20 vezes mais sensíveis que roedores. Isto resulta numa DL50 para humanos de 1,6 mg/kg quando DMT é administrada por via intravenosa, ou seja, 112 mg para uma pessoa padrão de 70 kg. A biodisponibilidade de uma substância administrada via intravenosa é assumida como 100%. A biodisponibilidade de uma dose por via oral é significantemente menor. Assume-se, então o fator de conversão da biodisponibilidade intravenosa para oral como 1:5 baseado na suposição que 0,4 mg/kg por via intravenosa ser equivalente a aproximadamente 2,0 mg/kg por via oral. Assim, estima-se, que por via oral a DL50 seja de 8 mg/kg, concluindo-se que uma dose letal de ayahuasca em seres humanos, é provavelmente maior que 20 vezes a dose típica cerimonial (Gable, 2007).
Quanto às β-carbolinas, parece que estas não são potencialmente tóxicas, uma vez que a DL50 em ratos é de 120mg/kg. Autópsias de bovinos que consumiram grandes quantidades de arbustos que contém harmalina demonstraram somente congestão passiva visceral (Laing & Siegel, 2003).
Estudos realizados em camundongos mostram que as β-carbolinas produzem efeitos na temperatura corpórea e na função motora, aumentando a intensidade de tremores de forma dose-dependente, efeitos que parecem envolver mecanismos serotoninérgicos, noradrenérgicos e GABAérgicos (Freedland & Mansbach, 1999).
Em relação aos estudos de toxicidade aguda e crônica da exposição à ayahuasca por humanos, Grob et al. (1996) não verificaram evidências de efeitos adversos graves em voluntários que usavam ayahuasca em cerimônias religiosas. Neste contexto, o chá é consumido regularmente por homens e mulheres na faixa de idade dos 13 aos 90 anos. A avaliação psicológica de usuários de longo prazo não encontrou evidências de prejuízos nas atividades mentais. Funções cognitivas, fluência verbal, habilidade matemática, motivação, bem-estar emocional e personalidade foram alguns dos parâmetros avaliados no estudo. De fato, tem sido reportado que vários usuários regulares de ayahuasca com idade aproximada de 80 anos e que fizeram uso desde sua adolescência, permaneceram com acuidade mental e vigor físico preservados (Callaway et al., 1999).
No estudo conduzido por Callaway et al. (1994), observou-se que não há evidências de dependência física, mas alguma tolerância pode ser desenvolvida com o uso regular, sendo que podem ocorrer alterações nos níveis de neurotransmissores, principalmente da serotonina.
Efeitos adversos à saúde podem ocorrer a partir do uso casual da ayahuasca, particularmente quando substâncias serotoninérgicas são utilizadas em conjunto. É fato que a DMT pode induzir episódios psicóticos transitórios, que, no entanto, se resolvem espontaneamente em algumas horas. Até o momento não houve estudos conclusivos de que a ayahuasca possua potencial de abuso substancial ou persistente. Por outro lado, vem sendo registrados os benefícios psicológicos em longo prazo dentro de um uso contextualmente religioso, sendo que se têm observado que os usuários dedicados, com o tempo perdem o interesse pelo álcool, tabaco, cocaína entre outras substâncias (Gable, 2007). A ayahuasca tem sido sugerida como adjunto no tratamento da dependência ao álcool e outras drogas de abuso (Grob et al., 1996; McKenna, 2004;). A margem de segurança da utilização da ayahuasca em uma cerimônia religiosa se compara ao uso da codeína, mescalina ou metadona. O potencial de dependência oral do DMT e perturbação psicológica são mínimas de acordo com Gable (2007).
A DMT aumenta rapidamente os batimentos cardíacos, bem como a pressão sistólica e diastólica. Estudos com administração oral de β-carbolinas juntamente com DMT, induziram a um aumento dos picos dos batimentos cardíacos e pressão arterial cerca de um terço a mais que quando a DMT é administrada isoladamente após 90 e 120 minutos. Como dito anteriormente, as β-carbolinas contribuem para o aumento da quantidade de serotonina na fenda sináptica. O acúmulo excessivo pode produzir uma série de efeitos adversos, tais como tremor, diarréia, instabilidade autonômica, hipertermia, sudorese, espasmos musculares e possivelmente morte. Esse conjunto de sinais e sintomas é conhecido como síndrome serotoninérgica. Efeitos colaterais como desconforto físico ou dor crônica podem ser exacerbados pela ayahuasca (Callaway et al., 1999; Gable, 2007).
De fato, somente um caso de intoxicação fatal foi registrado depois de suposta ingestão da ayahuasca por um homem branco de 25 anos de idade. Análises macro e microscópicas não foram conclusivas, revelando somente congestão e edema tecidual. A análise toxicológica revelou as seguintes concentrações sanguíneas na vítima: DMT (0,02 mg/L); 5-metoxi-N,N-dimetiltriptamina (1,88 mg/L); THH (0,38 mg/L); HRL (0,07 mg/L) e HRM (0,17 mg/L). A causa da morte apontada pelo médico legista foi intoxicação alucinógena por aminas (Sklerov et al., 2005). Em contrapartida, essa publicação foi contestada por Callaway et al. (2006), que relata que nenhuma mistura de plantas, tradicionalmente usadas em cultos de tribos indígenas concentraria quantidade suficiente de 5-metoxi-N,Ndimetiltriptamina para levar a óbito um ser humano. Aventa a hipótese de que a pessoa em questão poderia ter ingerido além do chá, a substância sintética, o que poderia justificar as altas concentrações encontradas no sangue do jovem. Outra possibilidade seria a de se ter confundido a DMT que é o componente usual da ayahuasca com o seu análogo 5-metoxiN,N-dimetiltriptamina que possui um potencial tóxico muito mais relevante e significativo.
CONSIDERAÇÕES FINAIS
A utilização da ayahuasca é uma polêmica que ainda carece de vários estudos farmacocinéticos, farmacodinâmicos e toxicológicos para que se consiga chegar a um consenso de seu uso com segurança. Em paralelo, o quadro que se apresenta é de um número cada vez maior de adeptos, aparentemente indiferentes ao risco de se fazer uso regular de uma bebida que pode ter efeitos benéficos conforme apresentado, mas dos quais não se sabe quais efeitos indesejáveis podem vir a ser manifestados em longo prazo.
O fato de os usuários terem somente depoimentos favoráveis à ingestão não deve ser usado como justificativa para se interromper os estudos ao redor da ayahuasca, muito pelo contrário, devem servir de incentivo para que se verifique se realmente os efeitos benéficos apontados são condizentes com a realidade e podem ser utilizados no combate à farmacodependência e até mesmo da reinserção de indivíduos na sociedade.
O uso do chá por grávidas e crianças deve ser outro fator a ser considerado com mais critério, uma vez que em ambas as situações o organismo responde de forma diferenciada. No caso de mulheres grávidas, é ainda mais delicado, uma vez que a exposição à ayahuasca nesse período pode promover efeitos tóxicos no feto durante seu desenvolvimento.
No entanto, mesmo com a escassez de informações sobre a segurança de seu uso, sem dados científicos que indiquem seus riscos à saúde, não se pode deixar de reconhecer a importância de seu uso associado à religiosidade e ao seu contexto histórico-cultural brasileiro.
REFERÊNCIAS
Aranha C, Travaine G, Correa MA. Aspectos botânicos e taxonômicos das plantas Banisteriopsis sp e Psychotria sp. 1º Congresso em Saúde. Centro de Estudos Médicos – União do Vegetal; 1991 Maio 30-Jun 02; São Paulo, Brasil.
Barker SA, Littlefield-Chaubaud MA, David, C. Distribution of the hallucinogens N,N-dimethyltryptamine and 5-methoxyN,N-dimethyltryptamine in rat brain following intraperitoneal injection: application of a new solid-phase extraction LCAPcI-MS-MS isotope dilution method. J Chromatogr B 2001;751(1):37-47.
Blackledge RD, Taylor CM. Psychotria Viridis – A Botanical Source of Dimethyltryptamine (DMT). Microgram J. 2003; 1(1):18-22.
Brito GS. Farmacologia humana da hoasca (chá preparado de plantas alucinógenas usado em contexto ritual no Brasil). In: Labate BC. O uso ritual da ayahuasca. Campinas: Mercado de Letras Edições e Livraria; 2004. p.623-71.
Callaway JC, Airasksinen MM, Mckenna DJ, Brito GS, Grob CS. Platelet serotonin uptake sites increase in drinkers of ayahuasca. Psychopharmacology 1994; 116(1):385-7.
Callaway JC, Raymon LP, Hearn WL, Mckenna DJ, Grob,CS, Brito GS, Mash DC. Quantitation of N,Ndimethyltryptamine and harmala alkaloids in human plasma after oral dosing with ayahuasca. J Anal Toxicol. 1996;20(6):492-7.
Callaway JC, Grob CS, Ayahuasca preparations and serotonin reuptake inhibitors: a potential combination for severe adverse interactions. J Psychoactive Drugs 1998;30(4):367-9.
Callaway JC, Mckenna DJ, Grob CS, Brito GS, Raymon LP, Poland RE, et al. Pharmacokinetics of Hoasca alkaloids in healthy humans. J Ethnopharmacol. 1999;65(1):243-56.
Callaway JC, Grob CS, Mckenna DJ, Nichols DE, Shulgin A, Tupper KW. A demand for clarity regarding a case report on the ingestion of 5-methoxy-N,N-dimethyltryptamine (5-MeO-DMT) in an Ayahuasca preparation. J Anal Toxicol. 2006;29(1):406-7.
Carlini EA. Plants and central nervous system. Pharmacol Biochem Behav. 2003;75:501-12.
Cazenave SOS. Banisteriopsis caapi: ação alucinógena e uso ritual. Rev Psquiatr Clin. 2000;7(1):1-6.
Chauí M. Brasil: Mito fundador e sociedade autoritária. São Paulo: Fundação Perseu Abramo, 2000. 104p
Conselho Nacional Anti-Drogas. Resolução n.4, de 04 de novembro de 2004. Diário Oficial da União. Brasília (DF); 2004.
Costa, M.C.M., Figueiredo, M.C., Cazenave, S.O.S. Ayahuasca: Uma abordagem toxicológica do uso ritualístico. Rev Psquiatr Clin. 2005;32(6):310-8.
Cunningham, N. Hallucinogenic plants of abuse. Emerg Med Australas. 2008;20: 167-74.
Da Silveira DX, Grob CS, De Rios MD, Lopez E, Alonso LK, Tacla C, et al. Ayahuasca in adolescence: a preliminary psychiatric assessment. J Psychoactive Drugs 2005;37(2):129-33.
Doering-Silveira E, Lopez E, Grob CS, De Rios MD, Alonso LK, Tacla C, et al. Ayahuasca in adolescence: a neuropsychological assessment. J Psychoactive Drugs 2005;37(2):123-8.
Doering-Silveira E, Grob CS, De Rios MD, Lopez E, Alonso LK, Tacla C, et al. Report on psychoactive drug use among adolescents using ayahuasca within a religious context. J Psychoactive Drugs 2005a;37(2):141-4.
Franzen F, Gross H. Tryptamine, N,N-dimethyltryptamine, N,N-dimethyl-5-hydroxytryptamine and 5- methoxytryptamine in human blood and urine. Nature 1965;21(1):84-93.
Freedland CS, Mansbach RS. Behavioral profile of constituents in ayahuasca, an Amazonian psychoactive plant mixture. Drug Alcohol Depend. 1999; 54(1):183-94.
Gable RS. Risk assessment of ritual use of oral dimethyltryptamine (DMT) and harmala alkaloids. Addiction 2007;102(1):24-34.
Gambelunghe C, Aroni K, Rossi R, Moretti L, Bacci M. Identification of N,N-dimethyltryptamine and β-carbolines in psychotropic ayahuasca beverage. Biomed Chromatogr. 2008;22(1):1056-9.
Goulart SL. O contexto de surgimento do culto do Santo Daime: formação da comunidade e do calendário ritual. In: Labate BC. O uso ritual da ayahuasca. Campinas: Mercado de Letras Edições e Livraria; 2004. p.277-301.
Grob CS, Mckenna DJ, Callaway JC, Brito GS, Neves ES, Oberlaender G, et al. Human Psychopharmacology Of Hoasca, A Plant Hallucinogen Used in Ritual Context in Brazil. J Nerv Ment Dis. 1996;184(2):86-94.
Goodman, L.S; Gilman, A. (eds.). As bases farmacológicas da terapêutica. 11.ed. Rio de Janeiro: Ed McGraw-Hill, 2007. 1848p.
Halpern JH, Pope HGJr. Do hallucinogens cause residual neuropsychological toxicity? Drug Alcohol Depend. 1999;53(3):247-56.
Jacob MS, Presti DE. Endogenous psychoactive tryptamines reconsidered: an anxiolytic role for dimethyltryptamine. Med Hypotheses 2005;64(1):930-7.
Labate BC. A literatura brasileira sobre as religiões ayahuasqueiras. In: Labate BC. O uso ritual da ayahuasca. Campinas: Mercado de Letras Edições e Livraria; 2004. p.231-73.
Labigaline EJ. O uso de Ayahuasca em um contexto religioso por ex-dependentes de álcool. [Dissertação] São Paulo: Escola Paulista de Medicina, UNIFESP; 1998.
Laing RR, Siegel JA. Hallucinogens: A forensic drug handbook. Boston: Academic Press; 2003. 290p.
Liwszyc GE, Vuori E, Rasanen I, Issakainen J. Daime – A ritual herbal potion. J Ethnopharmacol. 1992;36:91-2.
Luna LE. Vegetalismo:Shamanism among the mestizo population of the Peruvian Amazon. J Ethnopharmacol. 1986;11(1):123-33.
Mckenna, D, Towers, GHN, Abbott, F. Monoamino Oxidase inhibitors in South American Hallucinogenic Plants: Tryptamine and β-Carboline constituents of Ayahuasca. J Ethnopharmacol. 1984;10(1):195-223.
Mckenna D. Clinical investigations of the therapeutic potential of ayahuasca: rationale and regulatory challenges. Pharmacol Ther. 2004;102(1):111-29.
Nichols DE. Hallucinogens. Pharmacol Ther. 2004 101(2):131-81.
Ott J. Ayahuasca Analogues: Pangæan Entheogens. Washington: Natural Products Books Co.; 1994. 127p.
Pires APS, Oliveira CDR, Moura S, Dorr FA., Silva WA, Yonamine M. Gás Chromatographic Analysis of dimethyltryptamine and β-carboline alkaloids in ayahuasca, in Amazonian psychoactive plant beverage. J Phytochem Anal. 2009;20(2):149-53.
Pomilio AB, Vitale AA, Ciprian-Ollivier J, CetkovichBakmas M, Gómez R, Vázquez G. Ayahoasca: an experimental psychosis that mirrors the transmethylation hypothesis of schizophrenia. J Ethnopharmacol. 1999;65(1):29-51.
Riba J, Rodríguez-Fornells A, Urbano G, Morte A, Antonijoan R, Montero M, Callaway JC, et al. Subjective effects and tolerability of the South American psychoactive beverage Ayahuasca in healthy volunteers. Psycopharmacology 2001;154(1):85-95.
Riba J, Valle M, Urbano G, Yritia M, Morte A, Barbanoj MJ. Human pharmacology of ayahuasca: subjective and cardiovascular effects, monoamine metabolite excrection, and pharmacokinetics. J Pharmacol Exp Ther. 2003;306(1):73-83.
Santos, R.G., Moraes, C.C., Holanda, A. Ayahuasca e Redução do Uso Abusivo de Psicoativos: Eficácia Terapêutica? Psicol Teor Pesqui. 2006;22(3):363-70.
Shannon B. Os conteúdos das visões da Ayahuasca. MANA 2003;9(2):109-52.
Sklerov J, Levine B, Moore KA, King T, Fowler D. A fatal intoxication following the ingestion of 5-methoxy-N,Ndimethyltryptamine in an ayahuasca preparation. J Anal Toxicol. 2005;29(1):838-41.
Strassman RJ, Qualls CR. Dose-response study of N,Ndimethyltryptamine in humans. I. Neuroendocrine, autonomic, and cardiovascular effects. Arch Gen Psychiatry 1994;51(2):85-97.
Strassman RJ, Qualls CR, Uhlenhuth EH, Kellner R. Doseresponse study of N,N-dimethyltryptamine in humans. II. Subjective effects and preliminary results of a new rating scale. Arch Gen Psychiatry 1994;51(2):98-104.
Stuckey DE, Lawson R, Luna LE. EEG gamma coherence and other correlates of subjective reports during ayahuasca experiences. J Psychoactive Drugs 2005;37(2):163-78.
Thompson AC, Nicollier GF, Pope DF, Indolealkylamines of Desmanthus illinoensis and their growth inhibition activity. J Agric Food Chem. 1987;35(1):301-5.
Tupper, KW, Entheogens and existential intelligence: The use of plant teachers as cognitive tools. Can J Contin Med Educ. 2002;27(4):499-516.
Tupper, KW, The globalization of ayahuasca: Harm reduction or benefit maximization? Int J Drug Policy 2008;19(4):297-303.
Vorce SP, Sklerov JH. A general screening and confirmation approach to the analysis of designer tryptamines and phenethylamines in blood and urine using GC-EI-MS and HPLC-electrospray-MS. J Anal Toxicol. 2004;28(6):407-10.
Yritia M, Riba J, Ortuño J, Ramirez A, Castillo A, Alfaro Y, et al. Determination of N,N-dimethyltryptamine and β-carboline alkaloids in human plasma following oral administration of Ayahuasca. J Chromatogr B Analyt Technol Biomed Life Sci. 2002;779(1):271-81.
